Масштабные длительные клинические тесты продукта меполизумаб (mepolizumab), разработанного наикрупнейшим европейским фармпроизводителем GlaxoSmithKline, обосновали эффективность и сравнительную безопасность этого лекарства для нездоровых с томным течением эозинофильной формы астмы, приблизительно в два раза понижая частоту обострений и позволяя понизить пероральное применение кортикостероидов.
Эти характеристики меполизумаба, выявленные в процессе 2-ух предыдущих клинических испытаний препарата, проведенных на небольшом количестве пациентов, были подтверждены третьей фазой испытаний, проходившей с 9 ноября 2009 года по 5 декабря 2011 года. В ней приняли участие 621 астматик в возрасте от 12 до 74 лет с признаками эозинофильного воспаления и регулярными обострениями из 81 медицинского центра 13 стран мира.
В течение года с четырехнедельными интервалами всем участникам делали инъекции. 159 пациентам вводили плацебо, 154 — 75 граммов меполизумаба, 152 — 250 граммов, а 156 — 750 граммов этого препарата. Всего любой из участников испытаний получил по 13 внутривенных вливаний.
Результаты наикрупнейшго в этой области исследования, проведенного интернациональной командой ученых под управлением Йена Пэворда (Ian Pavord) из Лестерского института (Англия), 18 августа размещены в журнальчике The Lancet.
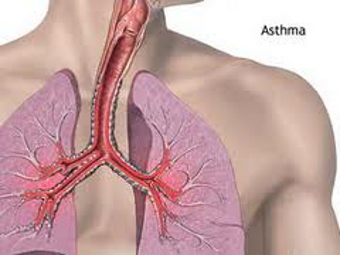
Приблизительно третья часть пациентов с тяжеленной бронхиальной астмой мучаются от ее эозинофильной формы, при которой наблюдается провоцируемое эозинофилами воспаление дыхательных путей и легких.
Меполизумаб, представляющий из себя моноклональное антитело к сенсору интерлейкина-5 (IL-5), биомаркера астмы, стимулирующего рост и активность эозинофилов, перекрывает выработку этих клеток и тем понижает частоту обострений заболевания.
По мнению авторов, это может свидетельствовать о том, что легочная функция и проявления симптоматики у пациентов с эозинофильной формой астмы не связаны с действием эозинофилов, против которых направлено действие меполизумаба, и требуют других методов лечения.
Наиболее частными побочными эффектами применения меполизумаба, отмеченными среди всех получавших препарат групп пациентов, были мигрени и воспаление слизистой оболочки носоглотки (назофарингит), однако авторы исследования расценивают их, как незначительные в сравнении с выявленными преимуществами.
Симона Хашимото (Simone Hashimoto) и Элизабет Бэл (Elisabeth Bel), специалисты из Амстердамского университета, комментируя полученные результаты, расценивают их как очень многообещающие для множества астматиков, лишенных в текущее время эффективных лекарств с незначительными побочными эффектами.По итогам испытаний выяснилось, что у пациентов из группы, получившей наибольшую дозу меполизумаба, было отмечено 52-процентное по сравнению с группой, получавшей плацебо, снижение количества обострений заболевания, что содержит в себе общее число астматических приступов, обращений к врачу и госпитализаций, также частоту применения кортикостероидных препаратов для купирования приступов.
У групп пациентов, получавших более низкие дозы меполизумаба, также отмечено резкое снижение частоты обострений по сравнению с плацебо-группой. Так, у больных, которым вводили по 75 граммов препарата, зарегистрировано 48-процентное снижение, а у членов группы, получавшей по 250 граммов лекарства — 39-процентное снижение.
В то же время авторами исследования было зафиксировано, что, несмотря на доказанную эффективность в отношении обострений астмы, меполизумаб не улучшает функцию легких, не снимает бронхиальную гиперреактивность и не уменьшает другие симптомы заболевания у пациентов из всех групп. Следующим шагом, по их мнению, должно стать направленное изучение стероидо-снижающих эффектов меполизумаба на большом сегменте пациентов, демонстрирующих зависимость от кортикостероидных препаратов, имеющих серьезные побочные эффекты.
GlaxoSmithKline уже около десяти лет изучает действие меполизумаба при различных, заболеваниях, связанных с эозинофилией. А именно, была доказана его неэффективность при атопическом дерматите и эффективность при гиперэозинофильном синдроме (ГЭС).
В США он был зарегистрирован в качестве орфанного препарата для лечения ГЭС под торговым названием Bosatria. В июле 2009 года GlaxoSmithKline направила заявку на получение для этого лекарства регистрационного удостоверения в Евросоюзе.
Медицина 2.0 (www.med2.ru)
Читайте также:
 Табак убьёт миллиард человек в следующие сто лет
Табак убьёт миллиард человек в следующие сто лет27-12-2012
Неутешительный прогноз делают учёные из Института Буффало (США): если не принять действенных мер,...
 Тяжелые астматики получили надежду на избавление от приступов
Тяжелые астматики получили надежду на избавление от приступов29-10-2012
Группа служащих Лейцестерского Института протестировала меполизумаб - новое средство, подавляющее...
 «Фермерские» бактерии защитят от астмы
«Фермерские» бактерии защитят от астмы20-08-2013
Как говорят ученые, детки, живущие в сельской местности и почаще контактирующие с микробами, менее...
 «Врачи без границ» расширили свою противотуберкулезную программу в Чечне
«Врачи без границ» расширили свою противотуберкулезную программу в Чечне21-02-2013
Интернациональная мед гуманитарная организация "Докторы без границ" Médecins Sans...
 Понижение смертности, сокращение числа больных фиброзно-кавернозным туберкулезом – одни из итогов реализации нацпроекта «
Понижение смертности, сокращение числа больных фиброзно-кавернозным туберкулезом – одни из итогов реализации нацпроекта «12-11-2013
За прошедшие с начала года 6 месяцев в Тамбовской области более чем на 2% возросла рождаемость,...





 Приближение ответственного события часто сопровождается проблемами со сном. Чем активнее попытки заставить себя ...
Приближение ответственного события часто сопровождается проблемами со сном. Чем активнее попытки заставить себя ...
 Когда кофе бодрит, а когда истощает. Всё о влиянии кофеина на мозг. Как он работает, где проходит грань пользы и вреда, ...
Когда кофе бодрит, а когда истощает. Всё о влиянии кофеина на мозг. Как он работает, где проходит грань пользы и вреда, ...
 Что делать, если препараты железа вызывают запор. Рассказываем про современные мягкие альтернативы и как лечить ...
Что делать, если препараты железа вызывают запор. Рассказываем про современные мягкие альтернативы и как лечить ...
 Практически каждый специалист предпочитает Стоматологические установки купить, которая бы полностью удовлетворяла ...
Практически каждый специалист предпочитает Стоматологические установки купить, которая бы полностью удовлетворяла ...